ГДЗ (ответы) Химия 10 класc Габриелян О.С. , Остроумов И.Г., Сладков С.А., 2019, §16 Сложные эфиры. Жиры
Во всех упражнениях красным цветом приводится решение, а фиолетовым ― объяснение. |
Какие вещества называют сложными эфирами?
Сложными эфирами называют производные карбоновых кислот, в которых атом водорода карбоксильной группы замещён углеводородным радикалом.
Как можно записать общую формулу жиров?
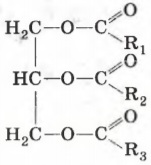 ,
,где R1, R2, R3 — радикалы, входящие в состав высших карбоновых кислот: масляной (―С3Н7), пальмитиновой (―С15Н31), стеариновой (―С17Н35), олеиновой (―С17Н33), линолевой (―С17Н31) и др.
Можно ли говорить о гомологических рядах жиров?
Нельзя, т.к. в состав жиров могут входить различные остатки как предельных, так и непредельных карбоновых кислот.
Задание 2
Что такое жиры?
Жиры ― это природные соединения, которые представляют собой сложные эфиры глицерина и высших карбоновых кислот.
Являются ли природные жиры индивидуальными химическими веществами?
Не являются, т.к. при выделении жиров получают и другие вещества.
Задание 3
Как физические свойства жиров зависят от природы углеводородного радикала, входящего в кислотный остаток?
В обычных условиях жиры, образованные остатками непредельных кислот, жидкие их называют еще маслами (кроме пальмового масла), а жиры, образованные остатками предельных кислот, твердые (кроме рыбьего жира).
Задание 4
Чему равна масса твёрдого мыла, полученного на основе 400 кг 40%-ного раствора гидроксида натрия и необходимого количества вещества тристеарата? Чему равно это количество?
Дано: m(раствора)=400 кг, ω(NaOH)=40%
Найти: m(C17H35COONa)-?
Решение
1-й способ
1. Рассчитываем массу гидроксида натрия в растворе:
m(NaOH)=ω(NaOH)•m(раствора):100%=40%•400 кг:100%=160 кг
2. Вычисляем количество вещества гидроксида натрия массой 160 кг по формуле: n=m/M, где M ― молярная масса.
Mr(NaOH)=40, поэтому M(NaOH)=40 кг/кмоль
n(NaOH)=m(NaOH)/M(NaOH)=160 кг : 40 кг/кмоль=4 кмоль
3. Составим химическое уравнение:
3NaOH + C3H5(C17H35COO)3 = C3H5(OH)3 + 3C17H35COONa
По уравнению реакции n(NaOH):n(C3H5(C17H35COO)3):n(C17H35COONa)=3:1:3, поэтому
n(C3H5(C17H35COO)3)=n(NaOH):3=4 кмоль:3=1,33 кмоль
n(C17H35COONa)=n(NaOH)=4 кмоль
4. Вычисляем массу мыла количеством вещества 4 кмоль по формуле: m=n•M, где M ― молярная масса.
M(C17H35COONa)=306 кг/кмоль
m(C17H35COONa)=n(C17H35COONa)•M(C17H35COONa)=4 кмоль • 306 кг/кмоль=1224 кг
2-й способ
1. Рассчитываем массу гидроксида натрия в растворе:
m(NaOH)=ω(NaOH)•m(раствора):100%=40%•400 кг:100%=160 кг
2. Составим химическое уравнение:
160 кг х кмоль у кг
3NaOH + C3H5(C17H35COO)3 = C3H5(OH)3 + 3C17H35COONa
120 кг 1 кмоль 918 кг
Над формулами соединений NaOH, C3H5(C17H35COO)3 и C17H35COONa записываем вычисленную массу гидроксида натрия (160 кг), неизвестные количество вещества тристеарата и массу мыла(х кмоль и у кг соответственно), а под формулами соединений ― массу соответствующего количества вещества и количество вещества согласно коэффициентам в химическом уравнении. Для этого вычисляем молярную массу веществ и, соответственно, массу 3 кмоль гидроксида натрия и 3 кмоль мыла, т.к. с 3 кмоль NaOH и 1 кмоль C3H5(C17H35COO)3 образуется 3 кмоль C17H35COONa.
M(NaOH)=40 кг/кмоль, масса 1 кмоль=40 кг, а масса 3 кмоль=120 кг
M(C17H35COONa)=306 кг/кмоль, масса 1 кмоль=306 кг, а масса 3 кмоль=918 кг
х=n(C3H5(C17H35COO)3)=160 кг • 1 кмоль : 120 кг=1,33 кмоль
х=m(C17H35COONa)=918 кг • 160 кг : 120 кг=1224 кг
Ответ: 1224 кг мыла и 1,33 кмоль тристеарата
Задание 5
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
этиловый спирт ⟶ ацетальдегид ⟶ уксусная кислота ⟶ метиловый эфир уксусной кислоты ⟶ ацетат калия.
2C2H5OH + CuO ⟶ CH3CHO + Cu + H2O
CH3CHO + Ag2O ⟶ CH3COOH + 2Ag↓
CH3OH + CH3COOH ⇄ CH3COOCH3 + H2O
CH3COOCH3 + KOH ⟶ CH3COOK + CH3OH
Задание 6
У какого из обитателей морей толщина подкожного жира достигает 1 м? В китов.
У кого из морских млекопитающих самое жирное молоко (40% жира)? В дельфинов.
Объясните биологическую целесообразность данных явлений. В случае затруднения используйте Интернет.
Подкожный жировой слой выполняет несколько функций:
― защищает от переохлаждения (терморегуляция);
― создается энергетический запас;
― удерживается вода в организме;
― защита от механического воздействия;
― обеспечение плавучести.
Благодаря жирности молока его поверхностное натяжение в 30 раз больше, чем воды, что особенно важно, учитывая кормление под водой (струя молока не расплывается в воде).
ЛАБОРАТОРНЫЙ ОПЫТ смотри здесь...
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети