ГДЗ (ответы) Химия 10 класc Габриелян О.С. , Остроумов И.Г., Сладков С.А., 2019, §17 Углеводы
Во всех упражнениях красным цветом приводится решение, а фиолетовым ― объяснение. |
Какие вещества называют углеводами?
Углеводы ― органические соединения, состоящие из одной или нескольких молекул простых сахаров (многоатомных альдегидо- или кетоноспиртов).
Углеводы ― органические соединения с общей формулой Cm(H2O)n, где m, n ≥ 3.
Предложите признак, на основании которого этот тип веществ можно разделить на классы. Назовите эти классы и приведите примеры представителей каждого из них.
По числу остатков моносахаридов в молекуле углеводы разделяют на моносахариды (глюкоза C6H12O6, фруктоза C6H12O6, галактоза C6H12O6, рибоза C5H10O5, дезоксирибоза C5H10O4), олигосахариды (сахароза, мальтоза, лактоза), полисахариды (крахмал, целлюлоза, гликоген).
По способности гидролизоваться углеводы разделяют на моносахариды (глюкоза, фруктоза, галактоза), дисахариды (сахароза, мальтоза, лактоза), полисахариды (крахмал, целлюлоза, гликоген, хитин).
Моносахариды содержат 1 моносахаридный остаток, олигосахариды ― от 2 до 10 моносахаридных остатков, а полисахариды ― от 10 до 5000 моносахаридных остатков.
Задание 2
Почему глюкозу относят к соединениям с двойственной функцией?
Глюкоза проявляет характерные свойства двух разных класов органических соединений, т.к. является одновременно и многоатомным спиртом, и альдегидом, то есть альдегидоспиртом.
Ответ подтвердите уравнениями химических реакций.
Глюкоза, как многоатомный спирт, взаимодействует со свежеполученным осадком гидроксида меди (II) с растворением осадка и образованием ярко-синего раствора сахарата меди (II).
Глюкоза, как альдегид, при нагревании со свежеполученным осадком гидроксида меди (II) дает осадок красного цвета оксида меди (I):
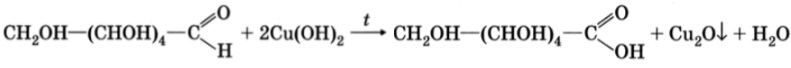
Глюкоза, как альдегид, с аммиачным раствором оксида серебра (I) при небольшом нагревании дает реакцию "серебряного зеркала":
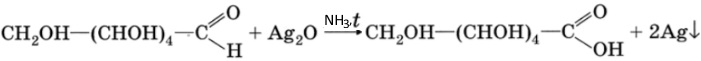
Задание 3
Какие вещества называют дисахаридами?
Дисахариды ― углеводы, состоящие из двух остатков моносахаридов.
Приведите примеры. Cахароза, лактоза, мальтоза.
Задание 4
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) крахмал ⟶ глюкоза ⟶ сорбит;
(C6H10O5)n + nH2O ⟶ nC6H12O6
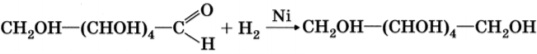
б) глюкоза ⟶ глюконовая кислота ⟶ глюконат кальция;
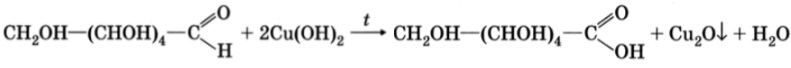
2CH2OH―(CHOH)4―COOH + Ca(OH)2 ⟶ (CH2OH―(CHOH)4―COO)2Ca + 2H2O
в) глюкоза ⟶ этиловый спирт ⟶ этиловый эфир уксусной кислоты.
C6H12O6дрожжи⟶ 2C2H5OH + 2CO2↑
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O
Задание 5
Сравните состав, строение, физические и химические свойства крахмала и целлюлозы.
Крахмал и целлюлоза состоят из полисахаридов, и имеют одинаковую молекулярную формулу (C6H10O5)n.
Молекулы крахмала имеют как линейное, так и разветвленное строение, а целлюлозы ― только линейное строение. Степень полимеризации макромолекул крахмала меньше, чем у целлюлозы.
Крахмал ― порошок белого цвета, зёрна которого набухают в горячей воде с образованием крахмального клейстера, а целлюлоза ― порошок белого цвета, не растворяется в воде и не набухает даже в горячей.
В отличие от целлюлозы крахмал дает синюю окраску при взаимодействии с иодом (качественная реакция на крахмал).
Целлюлоза значительно труднее подвергается гидролизу, чем крахмал.
(C6H10O5)n + nH2O → nC6H12O6
Задание 6
Рассчитайте объём углекислого газа (н.у.), который выделяется при спиртовом брожении 200 кг 9%-ного раствора глюкозы. Какая масса этилового спирта при этом получится?
Дано: m(раствора)=200 кг, ω(C6H12O6)=9%
Найти: V(CO2)-?, m(C2H5OH)-?
Решение
1-й способ
1. Рассчитываем массу глюкозы в растворе:
m(C6H12O6)=ω(C6H12O6)•m(раствора):100%=9%•200 кг:100%=18 кг
2. Вычисляем количество вещества глюкозы массой 18 кг по формуле: n=m/M, где M ― молярная масса.
Mr(C6H12O6)=180, поэтому M(C6H12O6)=180 кг/кмоль
n(C6H12O6)=m(C6H12O6)/M(C6H12O6)=18 кг : 180 кг/кмоль=0,1 кмоль
3. Составим химическое уравнение:
C6H12O6 ⟶ 2C2H5OH + 2CO2↑
По уравнению реакции n(C6H12O6):n(C2H5OH):n(CO2)=1:2:2, поэтому
n(C2H5OH)=n(CO2)=2•n(C6H12O6)=2•0,1 кмоль=0,2 кмоль
4. Вычисляем объём углекислого газа количеством вещества 0,2 кмоль по формуле: V=n•VM, где VM=22,4 м3/кмоль ― молярный объём.
V(CO2)=n(CO2)•VM=0,2 кмоль • 22,4 м3/кмоль=4,48 м3
5. Вычисляем массу этилового спирта количеством вещества 0,2 кмоль по формуле: m=n•M, где M ― молярная масса.
M(C2H5OH)=46 кг/кмоль
m(C2H5OH)=n(C2H5OH)•M(C2H5OH)=0,2 кмоль • 46 кг/кмоль=9,2 кг
2-й способ
1. Рассчитываем массу глюкозы в растворе:
m(C6H12O6)=ω(C6H12O6)•m(раствора):100%=9%•200 кг:100%=18 кг
2. Составим химическое уравнение:
18 кг х кг у м3
C6H12O6⟶ 2C2H5OH + 2CO2↑
180 кг 92 кг 44,8 м3
Над формулами соединений C6H12O6, C2H5OH и CO2 записываем вычисленную массу глюкозы (18 кг) и неизвестные массы этилового спирта и объём углекислого газа (х кг и у м3 соответственно), а под формулами соединений ― массу и объём соответствующего количества вещества согласно коэффициентам в химическом уравнении. Для этого вычисляем молярную массу веществ и, соответственно, массу 1 кмоль глюкозы и массу 2 кмоль этилового спирта, так как с 1 кмоль глюкозы C6H12O6 образуется 2 кмоль этилового спирта C2H5OH и 2 кмоль углекислого газа CO2 (1 кмоль любого газа при н.у. занимает объем 22,4 м3, а 2 кмоль ― в 2 раза больший объём, т.е. 44,8 м3).
M(C6H12O6)=180 кг/кмоль, масса 1 кмоль=180 кг
M(C2H5OH)=46 кг/кмоль, масса 1 кмоль=46 кг, а масса 2 кмоль=92 кг
х=m(C2H5OH)=92 кг • 18 кг : 180 кг=9,2 кг
у=V(CO2)=18 кг • 44,8 м3 : 180 кг=4,48 м3
Ответ: при спиртовом брожении 200 кг 9%-ного раствора глюкозы получилось 18 кг этилового спирта и выделилось 4,48 м3 углекислого газа.
Задание 7 Целлюлоза используется в пищевой промышленности как добавка, препятствующая слёживанию и комкованию порошкообразных продуктов (код E460). Под действием соляной кислоты в желудке человека примерно 5% целлюлозы гидролизуется. Какая масса глюкозы получится при гидролизе из 8,1 г полисахарида?
Дано: mпракт.((C6H10O5)n)=8,1 г, η((C6H10O5)n)=5%
Найти: m(C6H12O6)-?
Решение
1-й способ
1. Рассчитываем массу целлюлозы, которая практически гидролизуется:
m((C6H10O5)n)=ω((C6H10O5)n)•mпракт.((C6H10O5)n):100%=5%•8,1 г:100%=0,405 г
2. Вычисляем количество вещества целлюлозы массой 0,405 г по формуле: n=m/M, где M ― молярная масса.
Mr((C6H10O5)n)=162n, поэтому M((C6H10O5)n)=162n г/моль
n((C6H10O5)n)=m((C6H10O5)n)/M((C6H10O5)n)=0,405 г : 162n г/моль=0,0025/n моль
3. Составим химическое уравнение:
(C6H10O5)n + nH2O → nC6H12O6↑
По уравнению реакции n((C6H10O5)n):n(C6H12O6)=1:n, поэтому
n(C6H12O6)=n•n((C6H10O5)n)=n•0,0025/n моль=0,0025 моль
4. Вычисляем массу глюкозы количеством вещества 0,0025 моль по формуле: m=n•M, где M ― молярная масса.
M(C6H12O6)=180 г/моль
m(C6H12O6)=n(C6H12O6)•M(C6H12O6)=0,0025 моль • 180 г/моль=0,45 г
2-й способ
Рассчитываем массу целлюлозы, которая практически гидролизуется:
m((C6H10O5)n)=ω((C6H10O5)n)•mпракт.((C6H10O5)n):100%=5%•8,1 г:100%=0,405 г
2. Составим химическое уравнение:
0,405 г х г
(C6H10O5)n + nH2O → nC6H12O6↑
162n г 180n г
Над формулами соединений (C6H10O5)n и C6H12O6 записываем вычисленную массу целлюлозы (0,405 г) и неизвестную массу глюкозы (х г), а под формулами соединений ― массу соответствующего количества вещества согласно коэффициентам в химическом уравнении. Для этого вычисляем молярную массу веществ и, соответственно, массу 1 моль целлюлозы и массу n моль глюкозы, так как с 1 моль целлюлозы (C6H10O5)n образуется n моль глюкозы C6H12O6.
M((C6H10O5)n)=162n г/моль, масса 1 моль=162n г
M(C6H12O6)=180 г/моль, масса 1 моль=180 г, а масса n моль=180n г
х=m(C6H12O6)=0,405 г • 180n г : 162n г=0,45 г
Ответ: 0,45 г C6H12O6
ЛАБОРАТОРНЫЙ ОПЫТ смотри здесь...
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети