ГДЗ / ОТВЕТЫ Химия 8 класc Габриелян О.С. §18 Степень окисления
Красным цветом приводится решение, а фиолетовым ― объяснение. |
NO – оксид азота (II)
N2O5 – оксид азота (V)
N2O – оксид азота (I)
N2O3 – оксид азота (III)
NO2 – оксид азота (IV)
Объяснение.
Соединение оксид азота (II). Записываем химические символы элементов, а над ними валентность элементов: NIIОII. Наименьшее общее кратное валентностей обоих элементов равно два и делим его на величину валентности каждого из элементов (2:2=1 и 2:2=1) ― это индексы, которые ставим у символа соответствующего химического элемента (на письме 1 не пишем). Итак, формула NО
Соединение оксид азота (V). Записываем химические символы элементов, а над ними валентность элементов: NVОII. Наименьшее общее кратное валентностей обоих элементов равно десять и делим его на величину валентности каждого из элементов (10:5=2 и 10:2=5) ― это индексы, которые ставим у символа соответствующего химического элемента. Итак, формула N2О5
Соединение оксид азота (I). Записываем химические символы элементов, а над ними валентность элементов: NIОII. Наименьшее общее кратное валентностей обоих элементов равно два и делим его на величину валентности каждого из элементов (2:1=2 и 2:2=1) ― это индексы, которые ставим у символа соответствующего химического элемента (на письме 1 не пишем). Итак, формула N2О
Соединение оксид азота (III). Записываем химические символы элементов, а над ними валентность элементов: NIIIОII. Наименьшее общее кратное валентностей обоих элементов равно шесть и делим его на величину валентности каждого из элементов (6:3=2 и 6:2=3) ― это индексы, которые ставим у символа соответствующего химического элемента. Итак, формула N2О3
Соединение оксид азота (IV). Записываем химические символы элементов, а над ними валентность элементов: NIVОII. Наименьшее общее кратное валентностей обоих элементов равно четыре и делим его на величину валентности каждого из элементов (4:4=1 и 4:2=2) ― это индексы, которые ставим у символа соответствующего химического элемента (на письме 1 не пишем). Итак, формула NО2
Задание 2 Дайте названия бинарных соединений, формулы которых:
а) Cl2O7, Cl2O, ClO2;
Оксид хлора (VII), оксид хлора (I), оксид хлора (IV)
б) FeCl2, FeCl3;
Хлорид железа (II), хлорид железа (III)
в) MnS, MnO2, MnF4, MnO, MnCl4;
Сульфид марганца (II), оксид марганца (IV), фторид марганца (IV), оксид марганца (II), хлорид марганца (IV)
г) Сu2O, Mg2Si, SiCl4, Na3N, FeS.
Оксид меди (I), силицид магния, хлорид кремния (IV), нитрид натрия, сульфид железа (II)
Задание 3 Найдите по справочникам и словарям всевозможные названия веществ с формулами: а) CO2 и CO; б) SO2 и SO3. Объясните их этимологию. Дайте по два названия этих веществ по международной номенклатуре в соответствии с правилами, изложенными в параграфе.
Для СО2:
названия по международной номенклатуре СО2: диоксид углерода или оксид углерода (IV);
тривиальные названия: углекислый газ, двуокись углерода.
Для CO:
названия по международной номенклатуре: монооксид углерода или оксид углерода (II);
тривиальные названия: угарный газ.
Для SO2:
названия по международной номенклатуре: диоксид серы или оксид серы (IV);
тривиальные азвания: сернистый газ, сернистый ангидрид.
Для SO3:
названия по международной номенклатуре: триоксид серы или оксид серы (VI);
тривиальные названия: серный газ, серный ангидрид.
Задание 4 Какое ещё название можно дать аммиаку H3N? Нитрид водорода.
Задание 5 Найдите объём, который имеют при н у. 17 г сероводорода. Сколько молекул его содержится в этом объёме?
Дано: m(H2S)=17 г
Найти: V(H2S)-?, N(H2S)-?
Решение:
1-й способ
1. Количество вещества сероводорода массой 17 г рассчитываем по формуле: n=m/M, где M ― молярная масса.
M(H2S)=34 г/моль
n(Н2S)=m(Н2S)/M(Н2S)=17 г : 34 г/моль=0,5 моль
2. Объём сероводорода количеством вещества 0,5 моль рассчитываем по формуле: V=n•VM, где VM― молярный объём.
V(Н2S)=n(Н2S)•VM=0,5 моль • 22,4 л/моль=11,2 л
3. Число молекул сероводорода в количестве вещества 0,5 моль рассчитываем по формуле: N=n•NА, где NА― число Авогадро.
N(Н2S)=n(Н2S)•NА=0,5 моль • 6•1023 моль-1=3•1023 молекул
2-й способ
Сначала выведем формулы, которые мы будем использовать в этом упражнении.
Поставим в формулу V=n•VM выражение вычисления количества вещества заданной массы n=m/M, получим формулу: V=m•VM/M.
Поставим в формулу N=n•NA выражение вычисления количества вещества заданной массы n=m/M, получим формулу: N=m•NА/M.
1. Объём сероводорода массой 17 г рассчитываем по формуле: V=m•VM/M, где VM ― молярный объём.
M(H2S)=34 г/моль
V(Н2S)=m(Н2S)•VM:M(Н2S)=17 г • 22,4 л/моль : 34 г/моль=11,2 л
2. Число молекул сероворода в массе 17 г рассчитываем по формуле: N=m•NА/M, где NА ― число Авогадро.
N(Н2S)=m(Н2S)•NА:M(Н2S)=17 г • 6•1023 моль-1: 34 г/моль=3•1023 молекул
3-й способ
M(H2S)=34 г/моль
Для нахождения объёма сероводорода составляем пропорцию и решаем её:
34 г (1 моль) сероводорода занимают объём 22,4 л,
17 г сероводорода ― х л
х=22,4 л • 17 г : 34 г=11,2 л
Для нахождения числа молекул составляем пропорцию и решаем её:
в 34 г (1 моль) сероводорода содержится 6•1023 молекул Н2S,
в 17 г сероводорода ― х молекул Н2S
х=6•1023 • 17 : 34 =3•1023 молекул
Ответ: 17 г сероводорода при н.у. занимает объём 11,2 л и содержит 3•1023 молекул.
Задание 6 Вычислите массу 33,6 м3 метана CH4 при н. у. и определите число его молекул, содержащееся в этом объёме.
Дано: V(CH4)=33,6 м3
Найти: m(CH4)-?, N(CH4)-?
Решение:
1-способ
1. Количество вещества метана объёмом 33,6 м3 рассчитываем по формуле: n=V/VM, где VM ― молярный объём.
n(CH4)=V(CH4)/VM=33,6 м3 : 22,4 м3/кмоль=1,5 кмоль
2. Массу метана количеством вещества 1,5 кмоль рассчитываем по формуле: m=n•M, где M ― молярная масса.
M(CH4)=16 кг/кмоль
m(CH4)=n(CH4)•M(CH4)=1,5 кмоль • 16 кг/кмоль=24 кг
3. Число молекул метана в количестве вещества 1,5 кмоль рассчитываем по формуле: N=n•NА, где NА― число Авогадро.
N(CH4)=n(CH4)•NА=1,5 кмоль • 6•1026 кмоль-1=9•1026 молекул
2-й способ
Сначала выведем формулы, которые мы будем использовать в этом упражнении.
Поставим в формулу m=n•M выражение вычисления количества вещества заданного объёма n=V/VM, получим формулу: m=V•M/VM.
Поставим в формулу N=n•NA выражение вычисления количества вещества заданного объёма n=V/VM, получим формулу: N=V•NА/VM.
1. Массу метана объёмом 33,6 м3 вычисляем по формуле: m=V•M/VM, где VM ― молярный объём.
M(CH4)=16 кг/кмоль
m(CH4)=V(CH4)•M(CH4):VM=33,6 м3• 16 кг/кмоль : 22,4 м3/кмоль=24 кг
2. Число молекул метана в объёме 33,6 м3 рассчитываем по формуле: N=V•NА/VM, где NА ― число Авогадро.
N(CH4)=V(CH4)•NА:VM=33,6 м3 • 6•1026 моль-1: 22,4 м3=9•1026 молекул
3-й способ
M(CH4)=16 кг/кмоль
Для нахождения массы метана составляем пропорцию и решаем её:
объём 22,4 м3(1 кмоль) метана имеет массу 16 кг,
объём 33,6 м3 метана ― х кг
х=m(CH4)=33,6 м3 • 16 кг : 22,4 м3=24 кг
Для нахождения числа молекул составляем пропорцию и решаем её:
22,4 м3 (1 кмоль) метана содержат 6•1026 молекул СН4,
33,6 м3 метана ― х молекул СН4
х=N(CH4)=6•1026 • 33,6 м3 : 22,4 м3=9•1026 молекул
Ответ: 33,6 м3 метана CH4 при н.у. имеет массу 24 кг и содержит 9•1026 молекул.
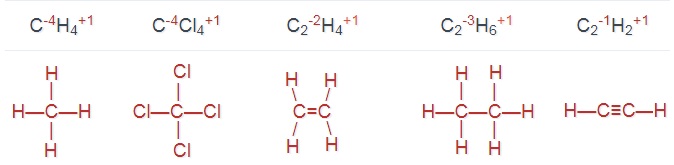
Задание 7 Определите степень окисления углерода и запишите структурные формулы следующих веществ, зная, что углерод в органических соединениях всегда четырёхвалентен: метана CH4, тетрахлорметана CCl4, этилена C2H4, этана C2H6, ацетилена C2H2.
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети