ГДЗ Химия 8 класc Рудзитис Г.Е., Фельдман Ф.Г., 2019, §22 Кислород, его общая характеристика, нахождение в природе и получение
Красным цветом приводится решение, а фиолетовым ― объяснение. |
Задание 2 Как получают кислород в лаборатории и в промышленности? Напишите уравнения соответствующих реакций.
Кислород в лаборатории получают из перманганата калия, пероксида водорода, бертоллетовой соли:
1) KMnO4 = K2MnO4 + MnO2 + O2↑ при нагревании
2) 2H2O2 MnO₂ = 2H2O + O2↑ при нагревании в присутствии катализатора оксида марганца (IV) MnO2
3) 2KClO3 = 2KCl + 3O2↑ при нагревании в присутствии катализатора оксида марганца (IV) MnO2
Кислород в промышленности получают из воздуха, который под давлением сжижают. Так как температура кипения жидкого азота (-196°С) ниже температуры кипения жидкого кислорода (-183°С), то азот испаряется, а жидкий кислород остается. Повторяя многократно процессы испарения и конденсации паров, удаётся полностью разделить жидкий воздух на азот и кислород.
Обсудите с соседом по парте, чем различаются эти способы.
В лаборатории кислород получают химическими реакциями, а в промышленности ― физическими методами разделения воздуха.
Задание 3 Какие вещества называют катализаторами?
Катализаторы – вещества, которые ускоряют химические реакции, но не расходующееся в процессе реакции.
Какой катализатор используют в известных вам реакциях получения кислорода.
Оксид марганца (IV) MnO2
Задание 4 Допишите уравнение реакции разложения оксида ртути (II) и расставьте необходимые коэффициенты.
2HgO = 2Hg + O2
Задание 5 Допишите уравнение реакции разложения пероксида водорода и расставьте необходимые коэффициенты.
2H2O2 = 2H2O + O2
Задание 6 Вычислите массовые доли элементов (в процентах):
а) в оксиде серы (IV);
Mr(SO2)=Ar(S)+2•Ar(O)=32+2•16=64
ω(S)=(Ar(S)/Mr(SO2))•100%=(32:64)•100%=50%
ω(О)=100%-ω(S)=100%-50%=50%
б) в бертоллетовой соли KClO3.
Mr(KClO3)=Ar(K)+Ar(Cl)+3•Ar(O)=39+35,5+3•16=122,5
ω(K)=(Ar(K)/Mr(KClO3))•100%=(39:122,5)•100%=31,9%
ω(Cl)=(Ar(Cl)/Mr(KClO3))•100%=(35,5:122,5)•100%=29%
ω(О)=100%-ω(K)-ω(Cl)=100%-31,9%-29%=39,1%
Задание 7 На основании закона сохранения массы веществ рассчитайте массу кислорода, вступившего в реакцию с 3,2 г меди, если в результате реакции образовалось 4 г оксида меди (II).
Дано: m(Сu)=3,2 г, m(CuО)=4 г
Найти: m(O2)-?
Решение
O2 + 2Cu = 2CuO
m(O2)=m(CuO)-m(Cu)=4 - 3,2=0,8 г
Ответ: 0,8 г
ТЕСТ 1
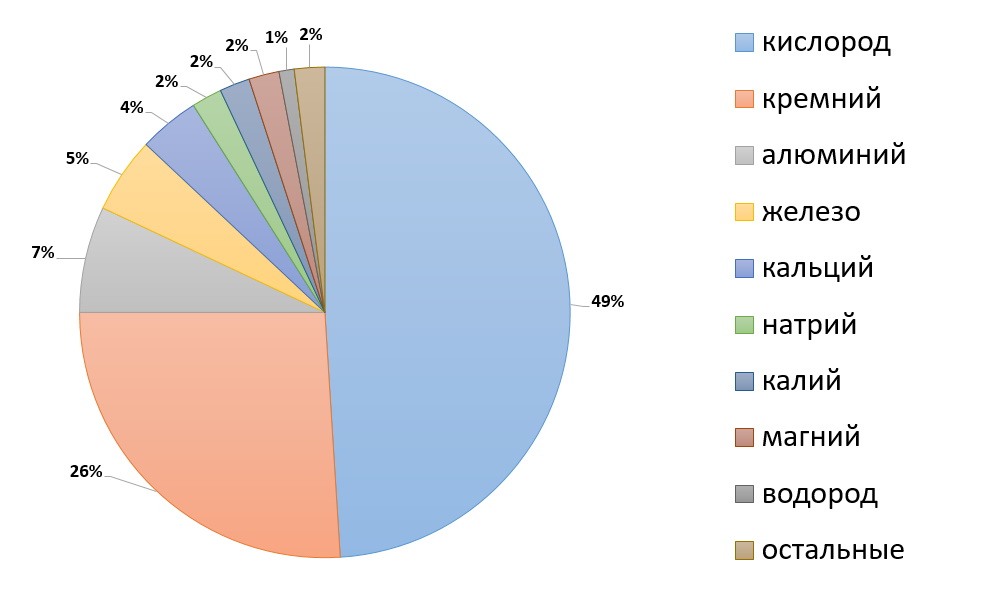
Самый распространённый химический элемент в земной коре – это
1) водород
2) кислород (49% по массе)
3) железо
4) кремний
Ответ: 2)
ТЕСТ 2
В предложении "Кислород входит в состав воздуха" речь идёт о кислороде
1) как о химическом элементе
2) как о простом веществе (О2)
Ответ: 2)
ТЕСТ 3
Укажите правую часть уравнения химической реакции разложения пероксида водорода H2O2.
1) 2H2 + 2O2
2) 2H2O + O2
3) H2O + H2
4) H2O + O2
Ответ: 2)
2H2O2 = 2H2O + O2
ТЕСТ 4
Для получения кислорода в лаборатории не используют вещество
1) KMnO4
2) KClO3
3) H2O2
4) CaO
Ответ: 4)
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети