ГДЗ к учебнику ХИМИЯ 8 КЛАСС Еремина и др. В.В. §11 Относительная атомная и молекулярная массы. Качественный и количественный состав вещества РЕШЕБНИК ОТВЕТЫ
Красным цветом приводится решение, а фиолетовым ― объяснение. |
Дайте определения понятий "относительная атомная масса", "относительная молекулярная масса".
Относительная атомная масса ― отношение массы атома данного химического элемента к 1/12 массы атома углерода. Относительная молекулярная масса показывает, во сколько раз масса молекулы больше 1/12 массы атома углерода.
Какой смысл имеет слово "относительная"? Слово «относительная» значит, что масса атома или молекулы определена сравнением с атомной единицей массы, т.к. относительный, тот что определяется в сопоставлении с чем-нибудь.
Задание 2
Что означает запись Ar(S) = 32? Атом серы в 32 раза тяжелее 1/12 атома углерода.
Задание 3
Какой атом тяжелее ― железа или кремния ― и во сколько раз? Атом железа тяжелее в 2 раза.
Ar(Fe)/Ar(Si)=56:28=2
Задание 4
Определите относительные молекулярные массы простых веществ: водорода, кислорода, хлора, меди, алмаза (углерода). Вспомните, какие из них состоят из двухатомных молекул, а какие ― из атомов.
Mr(H2)=2•Ar(H)=2•1=2
Mr(O2)=2•Ar(O)=2•16=32
Mr(Cl2)=2•Ar(Cl)=2•35,5=71
Mr(Cu)=Ar(Cu)=64
Mr(C)=Ar(C)=12
Задание 5
Рассчитайте относительные молекулярные массы следующих соединений: углекислого газа CO2, серной кислоты H2SO4, сахара C12H22O11, этилового спирта C2H5OH, мрамора CaCO3.
Mr(CO2)=Ar(C)+2•Ar(O)=12+2•16=44
Mr(H2SO4)=2•Ar(H)+Ar(S)+4•Ar(O)=2•1+32+4•16=98
Mr(C12H22O11)=12•Ar(C)+22•Ar(H)+11•Ar(O)=12•12+22•1+11•16=342
Mr(C2H5OH)=2•Ar(C)+6•Ar(H)+Ar(O)=2•12+6•1+16=46
Mr(CaCO3)=Ar(Ca)+Ar(C)+3•Ar(O)=40+12+3•16=100
Задание 6
В пероксиде водорода на один атом кислорода приходится один атом водорода. Определите формулу пероксида водорода, если известно, что её относительная молекулярная масса равна 34. Каково массовое соотношение водорода и кислорода в этом соединении?
Дано: HxOy, Mr(HxOy)=34
Найти: формулу HxOy-?, m(H):m(O)-?
Решение
Обозначим число атомов водорода через х, а число атомов кислорода через у, тогда соотношение атомов в формуле равно х:у=1:1, или х=у. С другой стороны Mr(HxOy)=x•Ar(H)+y•Ar(O)=x+16•y и по условию задачи x+16•y=34.
Составляем систему уравнений и решаем её:
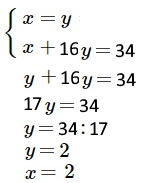
Следовательно, формула вещества H2O2
m(H):m(O)=(2•Ar(H)):(2•Ar(O))=(2•1):(2•16)=2:32=1:16
Ответ: H2O2, m(H):m(O)=1:16
Задание 7
Во сколько раз молекула углекислого газа тяжелее молекулы кислорода? В 1,375 раза.
Mr(CO2)=Ar(C)+2•Ar(O)=12+2•16=44, Mr(O2)=2•Ar(O)=2•16=32
Mr(CO2)/Mr(O2)=44:32=1,375
Задание 8
Что называют массовой долей химического элемента в соединении? Массовая доля химического элемента показывает, какая часть относительной молекулярной массы вещества приходится на данный элемент.
Задание 9
В каком массовом отношении нужно смешать железо и серу для получения сульфида железа FeS? 7:4
m(Fe):m(S)=Ar(Fe):Ar(S)=56:32=7:4
Задание 10
В каком массовом отношении нужно смешать алюминий и серу для получения сульфида алюминия Al2S3? 9:8
m(Al):m(S)=(2•Ar(Al)):(3•Ar(S))=(2•27):(3•32)=54:96=9:8
Определите массовые доли химических элементов в этом соединении.
Mr(Al2S3)=2•Ar(Al)+3•Ar(S)=54+96=150
ω(Al)=2•Ar(Al):Mr(Al2S3)=2•27:150=54:150=0,36, или 36%
ω(S)=3•Ar(S):Mr(Al2S3)=3•32:150=96:150=0,64, или 64%
Массовую долю серы можно найти еще так:
ω(S)=100%-ω(Al)=100%-36%=64%
Задание 11
Определите массовые доли серы и кислорода в молекуле SO2.
Mr(SO2)=Ar(S)+2•Ar(O)=32+2•16=64
ω(S)=Ar(S):Mr(SO2)=32:64=0,5, или 50%
ω(O)=100%-ω(S)=100%-50%=50%
Задание 12
Определите массовые доли химических элементов в мраморе CaCO3.
Mr(CaCO3)=Ar(Ca)+Ar(C)+3•Ar(O)=40+12+3•16=100
ω(Ca)=Ar(Ca):Mr(CaCO3)=40:100=0,4, или 40%
ω(C)=Ar(C):Mr(CaCO3)=12:100=0,12, или 12%
ω(O)=100%-ω(Ca)-ω(C)=100%-40%-12%=48%
Задание 13
Рассчитайте массу атомов кислорода в куске мрамора CaCO3 массой 20 г.
Дано: m(CaCO3)=20 г
Найти: m(O)-?
Решение
1-й способ
Mr(CaCO3)=Ar(Ca)+Ar(C)+3•Ar(O)=40+12+3•16=100
ω(O)=3•Ar(O):Mr(CaCO3)=3•16:100=0,48
m(O)=ω(O)•m(CaCO3)=0,48•20 г=9,6 г
2-й способ
Mr(CaCO3)=Ar(Ca)+Ar(C)+3•Ar(O)=40+12+3•16=100
ω(O)=3•Ar(O):Mr(CaCO3)=3•16:100=0,48, или 48%
Масу атомов кислорода вычисляем с помощью пропорции:
в 100 г CaCO3 содержится 48 г атомов O, а
в 20 г CaCO3 ― х г атомов O
100 г : 20 г = 48 г : х г, отсюда
х=48 г • 20 г : 100 г = 9,6 г
Ответ: m(O)=9,6 г
Задание 14
Установите формулу оксида азота, если его относительная молекулярная масса равна 46.
Дано: NxOy, Mr(NxOy)=46
Найти: формулу NxOy−?
Решение
Mr(NxOy)=x•Ar(N)+y•Ar(O)=14•x+16•y и по условию задачи 14•x+16•y=46
Поскольку не указано соотношение масс элементов, то задачу решим методом перебора.
Допустим, что x=y=1, тогда 14•1+16•1≠46, не подходит.
Допустим, что x=2 и у=1, тогда 14•2+16•1≠46, не подходит.
Допустим, что x=1 и y=2, тогда 14+16•2=46, следовательно, формула вещества NO2
Ответ: NO2
Задание 15
Неизвестное вещество состоит из трёх элементов ― углерода, водорода и кислорода. Относительная молекулярная масса вещества равна 30. Установите его формулу.
Дано: CxHyOz, Mr(CxHyOz)=30
Найти: формулу CxHyOz−?
Решение
Mr(CxHyOz)=x•Ar(C)+y•Ar(H)+z•Ar(O)=12•x+y+16•z и по условию задачи 12•x+y+16•z=30
Поскольку не указано соотношение масс элементов, то задачу решим методом перебора.
Допустим, что x=y=z=1, тогда 12+1+16≠30, не подходит.
Допустим, что x=1, y=2, z=1, тогда 12+2+16=30, следовательно, формула вещества CH2O
Ответ: CH2O
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети