ГДЗ (ответы) Химия 10 класc Габриелян О.С. , Остроумов И.Г., Сладков С.А., 2019, §12 Многоатомные спирты
Во всех упражнениях красным цветом приводится решение, а фиолетовым ― объяснение. |
Какие вещества называют многоатомными спиртами?
Многоатомными спиртами называются органические вещества, молекулы которых содержат две или более гидроксильные группы.
Напишите по две формулы и названия простейших представителей для двухатомных и трёхатомных спиртов.
Двухатомные спирты:
этиленгликоль, или этандиол-1,2 | пропандиол-1,3 |
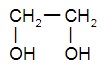 | 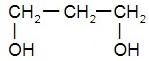 |
| глицерол, или пропантриол-1,2,3 | бутантриол-1,2,3 |
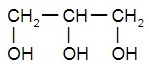 | 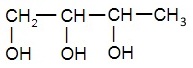 |
Какие свойства глицерина лежат в основе его применения? Гигроскопичность, сладкий вкус.
Гигроскопичность глицерина используют при изготовлении кремов для обуви; в кожевенном производстве и текстильной промышленности ― как смягчение кожи и придания эластичности тканям и пряжи; в парфюмерии и фармации ― как смягчающее средство или основу мазей, добавок к мылу, зубной пасте (чтобы предотвратить их высыхание). В пищевой промышленности глицерол используют как добавку к газированным напиткам и в кондитерских изделиях.
Задание 3
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) этанол ⟶ этен ⟶ 1,2-дихлорэтан ⟶ этандиол-1,2
CH3―CH2OH t,H₂SO₄⟶ H2C=CH2 + H2O
H2C=CH2 + Cl2 ⟶ CH2Cl―CH2Cl
CH2Cl―CH2Cl + 2NaOH ⟶ CH2OH―CH2OH+ 2NaCl
б) пропанол-1 ⟶ 1-бромпропан ⟶ пропен ⟶ пропандиол-1,2
CH3―CH2―CH2OH + HBr ⟶ CH3―CH2―CH2Br + H2O
CH3―CH2―CH2Br + NaOH C₂H₅OH⟶ CH3–CH=CH2 + NaBr + H2O
CH3–CH=CH2 + H2O кат.⟶ HO―CH2―CH(ОН)―CH3
Задание 4
Какой объём водорода (н.у.) выделится при взаимодействии 1,38 г натрия с избытком этиленгликоля?
Дано: m(Na)=1,38 г
Найти: V(H2)—?
Решение
1. Количество вещества натрия массой 1,36 г рассчитываем по формуле: n=m/M, где M ― молярная масса.
M(Na)=23 г/моль
n(Na)=m(Na)/M(Na)=1,36 г : 23 г/моль=0,06 моль
2. Составим химическое уравнение:
C2H4(OH)2 + 2Na ⟶ C2H4(ONa)2 + H2↑
По уравнению реакции n(Na):n(H2)=2:1, количество вещества водорода в 2 раза меньше количества вещества натрия, поэтому
n(H2)=n(C2H5OH):2=0,06 моль:2=0,03 моль
3. Вычисляем объём водорода в количестве вещества 0,03 моль по формуле: V=n•VM, где VM ― молярный объём.
n(H2)=n(H2)•VM=0,03 моль • 22,4 л/моль=0,672 л, или 672 мл.
Ответ: 672 мл
Задание 5
В двух пробирках находятся растворы этилового спирта и глицерина. Как их различить?
Качественной реакцией на глицерин (многоатомный спирт) является реакция взаимодействия со свежеполученным гидроксидом меди (II), в результате которой в пробирке с раствором глицерина осадок гидроксида меди (II) растворится и раствор окрасится в ярко-синий цвет. В пробирке с этиловым спиртом (одноатомный спирт) никаких изменений не произойдет.
Задание 6
К наступлению холодов в клеточной жидкости насекомых и некоторых земноводных резко увеличивается содержание глицерина. Объясните этот природный факт. Глицерин в клеточной жидкости выполняет роль природного антифриза, так как водный раствор глицерина замерзает (кристаллизируется) при гораздо более низкой температуре, чем вода (0°C) и предотвращает таким образом к наступлению холодов гибель этих насекомых.
Задание 8
Температура кристаллизации этиленгликоля ―13°C, температура кристаллизации воды 0°C. Попробуйте спрогнозировать температуру кристаллизации 50%-ного водного раствора этиленгликоля.
Можно было бы предположить, что температура кристаллизации 50%-ного водного раствора этиленгликоля равна среднему арифметическому значению температур: (―13°C + 0°C):2=―6,5°C.
Сравните ваш прогноз с истинным значением, найденным в Интернете.
Истинное значение температуры кристаллизации ―36°C.
Проанализируйте результат, сделайте выводы.
Смесь этиленгликоля и воды кристаллизуется при гораздо более низкой температуре, чем каждое из чистых веществ. Температура замерзания зависит от концентрации компонентов смеси.
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети