ГДЗ Химия 8 класc Габриелян О.С. §11 Взаимодействие атомов элементов-неметаллов между собой ОТВЕТЫ
Красным цветом приводится решение, а фиолетовым ― объяснение. |
Все элементы главной подгруппы VII группы (VIIА группы) Периодической системы Д.И. Менделеева (подгруппы фтора) образуют простые вещества, состоящие из двухатомных молекул. Запишите электронную схему образования и структурную формулу таких молекул, пользуясь общим химическим знаком для всей подгруппы Г (галоген).
Электронная схема: Г:Г
Структурная формула: Г―Г
Задание 2
Запишите схемы образования химических связей для веществ состав которых отображают формулами KCl и Cl2.
Схема образования ионной связи в KCl.
K0 -1e → K+
Cl0 +1e → Cl-
K0 + Cl0 → K+Cl-
Схема образования ковалентной неполярной связи в Cl2.
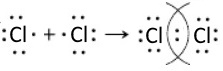
Задание 3
Сколько неспаренных электронов имеют атомы серы? Два
Сера ― элемент главной подгруппы VI группы, его атомы имеют по шесть электронов на внешнем уровне, среди них (8-6)=2 два неспаренных электрона.
Какая связь будет в молекулах S2? Ковалентная неполярная связь
Запишите схему образования химической связи в молекулах S2.
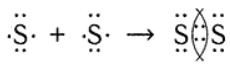
Задание 4
Расположите в порядке увеличения прочности химической связи вещества с формулами S2, Cl2, N2 и обоснуйте правильность своего решения. Чем больше общих электронных пар у атомов в молекуле (S=S, Cl―Cl, N≡N), тем прочнее связаны они друг с другом, поэтому прочность химической связи будет увеличиваться в ряду: Cl2, S2, N2
Как будет изменяться длина связи в молекулах составленного вами ряда? В ряду Cl2, S2, N2 увеличивается число общих электронных пар у атомов в молекулах, следовательно, прочнее связаны они друг с другом и расстояние между ядрами атома, которое называют длиной связи, уменьшается.
Задание 5
Разделите вещества на две группы по типу химической связи: N2, Li2O, KCl, O2, CaF2, H2.
| Формулы веществ с ковалентной неполярной связью | Формулы веществ с ионной связью |
| N2, O2, H2 | Li2O, KCl, CaF2 |
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети