ГДЗ (ответы) Химия 10 класc Габриелян О.С. , Остроумов И.Г., Сладков С.А., 2019, §7 Ароматические углеводороды, или арены
Красным цветом приводится решение, а фиолетовым ― объяснение. |
Какие углеводороды называют ароматическими? Ароматическими называют углеводороды, в молекулах которых содержится бензольное кольцо и которые имеют общую формулу CnH2n-6.
Приведите формулы трёх первых представителей гомологического ряда аренов.
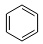 бензол |
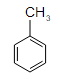 метилбензол |
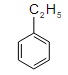 этилбензол |
Чем они различаются? Различные радикалы или их отсутствие.
Задание 2
Какие из перечисленных свойств соответствуют бензолу:
а) бесцветная жидкость;
б) бесцветный газ;
в) кристаллическое вещество;
г) без запаха;
д) с характерным запахом;
е) нерастворим в воде;
ж) легче воды;
з) тяжелее воды;
и) является хорошим растворителем;
к) очень ядовит?
Задание 3
Выведите молекулярную формулу углеводорода, молекулы которого содержат 92,31% углерода, а плотность его паров по водороду равна 39.
Дано: ω(C)=92,31%, или 0,9231, DH2(CxHy)=39
Найти: формула CxHy-?
Решение
DH2(CxHy)=M(CxHy)/M(H2), отсюда M(CxHy)=DH2(CxHy)•M(H2)=39•2 г/моль=78 г/моль
ω(H)=1-ω(C)=1-0,9231=0,0769
х=(ω(C)•M(CxHy)):M(C)=(0,9231• 78 г/моль):12 г/моль=6
y=(ω(H)•M(CxHy)):M(H)=(0,0769• 78 г/моль):1 г/моль=6
Ответ: формула углеводорода C6H6
Задание 4
Какие два вещества вступили в реакцию, если в результате образовались следующие продукты:
а) C6H5Cl и HCl;
C6H6 + Cl2кат.⟶ C6H5Cl + HCl
б) C6H5NO2 и H2O?
C6H6 + HNO3кат.⟶ C6H5―NO2 + H2O
Задание 5
Какой объём бензола (плотностью 0,9 г/мл) потребуется для получения 61 г нитробензола, если выход продукта реакции составляет 90%?
Дано: ρ(C6H6)=0,9 г/мл, mпракт.(C6H5NO2)=61 г, η(C6H5NO2)=90%
Найти: Vпракт.(C6H6)-?
Решение
1-й способ
1. Рассчитываем массу нитробензола теоретического.
mтеор.(C6H5NO2)=mпракт..(C6H5NO2):η(C6H5NO2)•100%=61 г : 90% • 100%=67,8 г
2. Количество вещества нитробензола рассчитываем по формуле: ʋ=m/M, где M ― молярная масса.
M(C6H5NO2)=123 г/моль
ʋ(C6H5NO2)=m(C6H5NO2)/M(C6H5NO2)=67,8 г : 123 г/моль=0,551 моль
3. Составляем химическое уравнение: C6H6 + HNO3 ⟶ C6H5NO2 + H2O
По уравнению реакции ʋ(C6H6):ʋ(C6H5NO2)=1:1, количества вещества одинаковые, поэтому:
ʋ(C6H6)=ʋ(C6H5NO2)=0,551 кмоль
4. Вычисляем массу бензола количеством вещества 1 моль по формуле: m=ʋ•M
M(C6H6)=78 г/моль
m(C6H6)=ʋ(C6H6)•M(C6H6)=0,551 моль • 78 г/моль=43 г
5. Вычисляем объём бензола:
V(C6H6)=m(C6H6)/ρ(C6H6)=43 г : 0,9 г/мл=38,7 мл
2-й способ
1. Рассчитываем массу нитробензола теоретического.
mтеор.(C6H5NO2)=mпракт..(C6H5NO2):η(C6H5NO2)•100%=61 г : 90% • 100%=67,8 г
1. Составляем химическое уравнение:
х г 67,8 г
C6H6 + HNO3 ⟶ C6H5NO2 + H2O
78 г 123 г
Над формулами соединений C6H6 и C6H5NO2 записываем неизвестную массу бензола (х г) и вычисленную массу нитробензола (67,8 г), а под формулами соединений ― массы количества вещества согласно коэффициентам в химическом уравнении.
M(C6H6)=78 г/моль, поэтому масса 1 моль=78 г
M(C6H5NO2)=123 г/моль, поэтому масса 1 моль=123 г
Массу бензола рассчитываем с помощью пропорции:
х г / 78 г = 67,8 г/ 123 г, отсюда
х=m(C6H6)=79 г • 67,8 г : 123 г=43 г
2. Вычисляем объём бензола:
V(C6H6)=m(C6H6)/ρ(C6H6)=43 г : 0,9 г/мл=38,7 мл
Ответ: V(C6H6)=47,8 мл
Задание 6
Какую массу бромбензола можно получить при бромировании 117 г бензола бромом массой 316 г? Какое из исходных веществ прореагирует не полностью и какова масса избытка этого вещества?
Дано: m(C6H6)=117 г, m(Br2)=316 г
Найти: m(C6H5Br)-?, mизб.(вещества)-?
Решение
1. Количество вещества бензола и брома рассчитываем по формуле: ʋ=m/M, где M ― молярная масса.
M(C6H6)=78 г/моль, M(Br2)=160 г/моль,
ʋ(C6H6)=m(C6H6)/M(C6H6)=117 г : 78 г/моль=1,5 моль
ʋ(Br2)=m(Br2)/M(Br2)=316 г : 160 г/моль=1,975 моль
2. Составляем химическое уравнение: C6H6+Br2 ⟶ C6H5Br+HBr
По уравнению реакции ʋ(C6H6)/1=ʋ(Br2)/1, подставив численные значения, получим 1,5/1<1,975/1 (1,5<1,975), следовательно, бром в избытке, то есть реагирует не полностью, поэтому расчеты будем проводить по данным бензола.
nизб.(Br2)=1,975-1,5=0,475 моль
По уравнению реакции ʋ(C6H6):ʋ(C6H5Br)=1:1, поэтому
n(C6H5Br)=n(C6H6)=1,5 моль
3. Массу бромбензола количеством вещества 1,5 моль рассчитываем по формуле: m=n•M.
M(C6H5Br)=157 г/моль
m(C6H5Br)=n(C6H5Br)•M(C6H5Br)=1,5 моль • 157 г/моль=235,5 г
4. Массу избытка брома количеством вещества 0,475 моль рассчитываем по формуле: m=n•M.
m(Br2)=n(Br2)•M(Br2)=0,475 моль • 160 г/моль=76 г
Ответ: mизб.(Br2)=76 г, m(C6H5Br)=235,5 г
Задание 7
Составьте и заполните обобщающую таблицу по теме "Углеводороды", в которой отразите следующие особенности классов этих органических соединений: состав, строение, способы получения, химические свойства, области применения.
Углеводороды | |||||
| Алканы | Алкены | Алкадиены | Алкины | Арены | |
| Состав | CnH2n+2 | CnH2n | CnH2n-2 | CnH2n-2 | CnH2n-6 |
| Строение | одинарные связи | одна двойная связь | две двойные связи | одна тройная связь | бензольное кольцо |
Химические свойства | |||||
| Реакция горения | + | + | + | + | + |
| Реакция гидратации | + | ||||
| Реакция гидрирования | + | + | + | ||
| Реакция дегидрирования | + | ||||
| Реакция галогенирования | + | + | + | + | + |
| Реакция гидрогалогенировани | + | + | + | ||
| Реакция полимеризации | + | + | |||
| Реакция изомеризации | + | ||||
| Крекинг | + | ||||
| Реакция нитрования | + | ||||
| Область применения | Являются сырьём для газо- и нефтехимических производств. | Этилен используется как сырьё для производства полиэтилена, галогенпроизводных, этилового спирта, этиленгликоля и других продуктов химической промышленности. | Являются сырьём для производства синтетических каучуков. | Ацетилен используется в производстве синтетических каучуков, поливинилхлорида и других полимеров, получают органические растворители, используют для газовой сварки и резки металлов. | Бензол используется в качестве сырья для синтетических красителей, ядохимикатов, синтетических моющих средств, лекарственных препаратов, пищевых добавок, пластмассы, взрывчатых веществ и многое другое. |
Похожие новости
Комментарии
Часто задаваемые вопросы
Для чего создан сайт?
Чтобы помочь ученикам.
У вас нет ГДЗ для моего учебника (
Это не проблема. Напиши нам чего нет и мы добавим.
Как с вами связатся?
Через почту: admin@gdz.cool или обратную связь.
Вам можно предложить учебник для ГДЗ?
Да. Отправь учебник на электронную почту, чтобы мы его решили.
В каком классе вы учитесь?
Социальные сети